Тофацитинібу цитрат — це рецептурний препарат (торгова назва Xeljanz), спочатку розроблений Pfizer для класу пероральних інгібіторів кінази Янус (JAK). Він може вибірково пригнічувати кіназу JAK, блокувати шляхи JAK/STAT і таким чином пригнічувати трансдукцію клітинного сигналу та експресію та активацію відповідних генів, що використовується для лікування ревматоїдного артриту, псоріатичного артриту, виразкового коліту та інших імунних захворювань.
Препарат містить три лікарські форми: таблетки, таблетки з уповільненим вивільненням і розчини для прийому всередину. Його таблетки були вперше схвалені FDA у 2012 році, а лікарську форму з уповільненим вивільненням було схвалено FDA в лютому 2016 року. Це перший засіб для лікування ревматоїдних суглобів. Ян є інгібітором JAK, який приймається перорально один раз на день. У грудні 2019 року було знову схвалено нове показання для препаратів із уповільненим вивільненням для лікування середнього та важкого активного виразкового коліту (ВК). Крім того, завершено поточну фазу 3 клінічних випробувань бляшкового псоріазу, і ще тривають шість клінічних випробувань фази 3, що включають активний псоріатичний артрит, ювенільний ідіопатичний артрит тощо. Тип показань. Переваги таблеток із уповільненим вивільненням, які мають тривалу дію і їх потрібно приймати лише один раз на день, сприяють лікуванню та контролю захворювань пацієнтів.
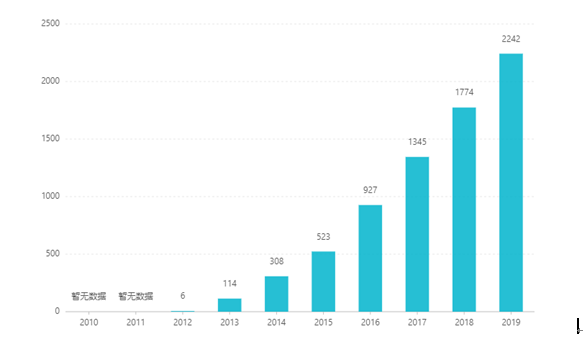
З моменту розміщення на біржі його продажі збільшувалися з року в рік, досягнувши 2,242 мільярда доларів США в 2019 році. У Китаї лікарську форму в таблетках було схвалено для продажу в березні 2017 року, а в 2019 році в результаті переговорів увійшла до каталогу медичного страхування категорії B. Останній виграш ставка становить 26,79 юанів. Однак через високі технічні бар’єри препаратів із уповільненим вивільненням ця лікарська форма ще не продається в Китаї.
Кіназа JAK відіграє важливу роль у запаленні, і було показано, що її інгібітори лікують певні запальні та аутоімунні захворювання. На сьогодні 7 інгібіторів JAK схвалено в усьому світі, включаючи Delgocitinib Leo Pharma, Fedratinib Celgene, упатініб AbbVie, Pefitinib Astellas, Baritinib Eli Lilly і Rocotinib Novartis. Проте лише тофацитиніб, барітиніб і рокотиніб схвалені в Китаї з перерахованих вище препаратів. Ми з нетерпінням чекаємо на те, що «Таблетки пролонгованого вивільнення Tofatib Citrate» Qilu будуть схвалені якнайшвидше та принесуть користь більшій кількості пацієнтів.
У Китаї в березні 2017 року NMPA схвалила оригінальне дослідження цитрату фацитибу для лікування дорослих пацієнтів з РА з недостатньою ефективністю або непереносимістю метотрексату під торговою назвою Shangjie. Згідно з даними Meinenet, продажі таблеток цитрату тофацітибу в державних медичних закладах Китаю в 2018 році становили 8,34 мільйона юанів, що було набагато нижче, ніж світові продажі. Значною частиною причин є ціна. Повідомляється, що початкова роздрібна ціна Shangjie становила 2085 юанів (5 мг*28 таблеток), а щомісячна вартість становила 4170 юанів, що є немалим тягарем для звичайних сімей.
Однак варто відзначити, що після переговорів у листопаді 2019 року Національна адміністрація медичного страхування включила tofacitib до «Національного базового медичного страхування, страхування від травм на виробництві та страхування материнства» на 2019 рік. Повідомляється, що щомісячна плата буде зменшена нижче 2000 юанів після узгодження ціни, що значно покращить доступність препарату.
У серпні 2018 року Комісія з повторної патентної експертизи Держінтелектуальної власності прийняла рішення про перегляд № 36902 запиту про визнання недійсним і визнала недійсним основний патент на Pfizertofatib, патент на сполуку, на підставі недостатнього розкриття специфікації. Однак термін дії патенту на кристалічну форму Pfizertofatiib (ZL02823587.8, CN1325498C, дата подання заявки 25.11.2002) закінчується у 2022 році.
База даних Insight показує, що, окрім оригінальних досліджень, п’ять генеричних препаратів Chia Tai Tianqing, Qilu, Kelun, Yangtze River і Nanjing Chia Tai Tianqing були схвалені для продажу у внутрішніх таблетованих формах тофацитинібу. Однак для таблеток із уповільненим вивільненням 26 травня заявку на маркетинг подала лише оригінальна дослідницька компанія Pfizer. Qilu стала першою вітчизняною компанією, яка подала заявку на маркетинг цієї форми. Крім того, CSPC Ouyi знаходиться на стадії випробування BE.
Changzhou Pharmaceutical Factory (CPF) є провідним фармацевтичним виробником API, готових рецептур у Китаї, який розташований у Чанчжоу, провінція Цзянсу. CPF було засновано в 1949 році. Ми присвятили себе Tofacitinib Citrate з 2013 року і вже представили DMF. Ми зареєструвалися в багатьох країнах і можемо надати вам найкращу підтримку документів для Tofacitinib Citrate.
Час публікації: 23 липня 2021 р